- Brook Jackson, un dénonciateur qui a travaillé sur l'étude de phase 3 de Pfizer sur le vaccin COVID, a déclaré que les données étaient falsifiées, que les patients n'avaient pas été aveuglés, que la société avait embauché du personnel mal formé pour administrer les injections et avait assuré le suivi de ceux signalés. Les effets secondaires restaient bien en deçà des attentes
- La FDA n'a pas enquêté sur la plainte de Jackson ni sur les allégations avant d'accorder la licence complète à la seringue Comirnaty de Pfizer.
- La FDA prévoit de passer 75 ans à évaluer les données sur lesquelles elle s'est appuyée pour accorder l'approbation complète de Comirnaty
- Un rapport sur les événements indésirables de Pfizer, couvrant la période de décembre 2020 à fin février 2021, montre que la seringue a causé des blessures graves, et souvent à long terme, non résolues
- Les données de Pfizer montrent également que la seringue cause de graves blessures aux femmes enceintes et allaitantes. Sur la base de ces seules données, connues de la FDA fin avril 2021, la seringue Pfizer aurait dû être retirée du marché.
Brook Jackson, un dénonciateur qui a travaillé sur l'étude de phase 3 de Pfizer sur le vaccin COVID à l'automne 2020, a déclaré que les données étaient falsifiées, que les patients n'avaient pas été aveuglés, que la société avait embauché du personnel mal formé pour administrer les injections et le suivi des effets indésirables signalés. réactions a été considérablement retardée.
Son témoignage a été publié dans le British Medical Journal le 2 novembre 2021 par le journaliste d'investigation Paul Thacker, qui a déclaré :
[Q] Pour les chercheurs qui ont testé le vaccin de Pfizer à plusieurs endroits au Texas cet automne, la vitesse a peut-être été au détriment de l'intégrité des données et la sécurité des patients l'a trouvée dépassée.
Le 2 décembre 2021, The Last American Vagabond a interviewé Jackson (vidéo ci-dessus) à propos de ce qu'elle a vu en travaillant sur l'étude Pfizer. Jackson est un auditeur d'essais cliniques formé avec plus de 15 ans d'expérience dans la coordination et la gestion de la recherche clinique.
Elle occupait auparavant un poste de directrice des opérations avant d'être embauchée début septembre 2020 par Ventavia Research Group, un organisme de recherche chargé de tester le vaccin COVID de Pfizer sur plusieurs sites au Texas. Dès le début, Jackson a remarqué à quel point l'opération était chaotique.
Compte tenu de la nouveauté de la technologie de transfert de gènes d'ARNm, elle a également trouvé la déclaration de consentement inadéquate. Elle a également constaté que l'ambulance contenait des médicaments périmés et que certains médicaments d'urgence essentiels devraient être complètement absents au cas où un participant subirait un événement indésirable aigu.
La falsification des données parmi les nombreux problèmes identifiés
Jackson affirme qu'elle a informé à plusieurs reprises ses superviseurs de la mauvaise gestion du laboratoire, des problèmes de sécurité des patients et des problèmes d'intégrité des données. Réalisant que ses préoccupations avaient été ignorées, elle a finalement déposé une plainte auprès de la Food and Drug Administration des États-Unis. Dans sa plainte auprès de la FDA, Jackson a énuméré une douzaine d'incidents préoccupants, dont les suivants :
- Les participants n'ont pas été surveillés par le personnel clinique après l'injection.
- Les patients qui ont présenté des effets indésirables n'ont pas fait l'objet d'une enquête rapide et les écarts de protocole n'ont pas été signalés.
- Les flacons d'injection de Pfizer ont été stockés à des températures inappropriées
- Les échantillons de laboratoire ont été étiquetés de manière incorrecte
Jackson a été libéré le même jour. Selon sa lettre de démission, la direction a décidé qu'elle "ne faisait pas partie de l'entreprise". Selon Jackson, c'était la première fois qu'elle était licenciée au cours de ses 20 ans de carrière en tant que coordinatrice de la recherche clinique. Comme Thacker le note :
Une rediffusion d'une réunion entre Jackson et deux administrateurs fin septembre 2020 a été entendue alors qu'un cadre de Ventavia a déclaré que la société n'était pas en mesure de quantifier le type et le nombre d'erreurs qu'elle a commises lors de l'examen de ses documents d'étude notés pour le contrôle qualité. À mon avis, c'est quelque chose de nouveau tous les jours, explique un responsable de Ventavia. Nous savons que c'est important.
Ventavia n'a pas répondu aux demandes de saisie de données, comme le montre un e-mail d'ICON, la société de recherche sous contrat avec laquelle Pfizer a travaillé sur l'étude. ICON a rappelé à Ventavia dans un e-mail daté de septembre 2020 : l'attente de cette étude est que toutes les demandes reçoivent une réponse dans les 24 heures.
ICON a ensuite marqué en jaune plus de 100 demandes en suspens datant de plus de trois jours. Cela incluait, par exemple, deux personnes à qui la personne testée a signalé des symptômes/réactions sévères… Selon le protocole, les personnes testées présentant des réactions locales de grade 3 doivent être contactées. Veuillez confirmer si un CONTACT NON PLANIFIÉ a eu lieu et mettre à jour le formulaire correspondant en conséquence.
Selon le protocole de l'étude, un contact téléphonique aurait dû être établi pour obtenir plus de détails et déterminer si une visite sur place est cliniquement indiquée. Les dossiers montrent que les problèmes duraient depuis des semaines.
Dans une liste de « mesures d'action » diffusée parmi les cadres de Ventavia début août 2020, peu de temps après le début de l'étude et avant l'embauche de Jackson, un cadre de Ventavia a nommé trois employés du site avec lesquels ils "ont eu le problème avec l'agenda électronique/le falsification de données, etc. » devrait discuter. L'un d'eux a été "exprimé verbalement de ne pas changer les dates et de ne pas noter les entrées tardives", selon une note.
Les révélations de Jackson ont récemment été présentées dans le documentaire italien "Pfizergate". Les documents qu'elle a collectés peuvent être téléchargés sur le site Web de COVID Vaccine Reaction.
Ventavia, Pfizer et la FDA ignorent les allégations
Curieusement, l'étendue des efforts de Ventavia pour se défendre consiste à nier que Jackson ait jamais travaillé sur l'étude Pfizer - une allégation qui s'est avérée fausse car elle possède des documents prouvant que c'est son travail qui a été commandé pour entreprendre l'étude.
Pfizer n'a pas non plus fait de commentaires à ce sujet. La société n'a répondu à aucune des questions du BMJ, notamment si les données de Ventavia ont été intégrées ou non dans les études d'innocuité et d'efficacité de Pfizer.
Nous savons cependant qu'aucun des problèmes soulevés par Jackson dans sa plainte auprès de la FDA n'a été mentionné ou traité dans le document d'information de Pfizer présenté au comité consultatif de la FDA le 20 décembre 2020, car la demande d'approbation d'urgence a été vérifiée.
La FDA a accordé une approbation d'urgence à la vaccination de Pfizer dès le lendemain malgré la réception de la plainte de Jackson, ce qui aurait dû remettre la FDA sur pied. Au moins, ils auraient dû enquêter sur la question avant de continuer.
Le BMJ a demandé une réponse de la FDA concernant les raisons pour lesquelles il n'a inspecté aucun des sites d'essai de Ventavia à la suite des allégations de Jackson, et s'il y a eu d'autres plaintes au sujet de l'étude. Un porte-parole de la FDA a déclaré au BMJ que l'agence ne pouvait pas commenter car il s'agissait d'une "question en cours", quoi que cela signifie.
Cependant, la FDA a déclaré qu'elle avait pleinement confiance dans les données utilisées pour l'approbation du vaccin COVID-19 de Pfizer-BioNTech et l'approbation de la commission. Étant donné qu'ils n'ont pas enquêté sur les plaintes de Jackson, leur vote de confiance ne me semble pas particulièrement convaincant.
D'autres témoins de Ventavia ont pris la parole
Jackson n'était pas le seul employé de Ventavia à être licencié après avoir fait part de ses inquiétudes quant à l'intégrité de l'étude de Pfizer. Plusieurs autres employés de Ventavia sont partis ou ont été licenciés, a déclaré Thacker. Parmi eux se trouve un responsable de Ventavia qui a assisté à la réunion susmentionnée fin septembre. Thacker écrit :
Dans un SMS envoyé [à Jackson] en juin, l'ancien officier s'est excusé et a déclaré que "tout ce dont vous vous êtes plaint était exact". Deux anciens employés de Ventavia ont parlé anonymement au BMJ, craignant des représailles et la perte d'emplois dans la communauté de recherche très unie. Les deux ont confirmé des aspects généraux de la plainte de Jackson.
L'une d'entre elles a déclaré qu'au cours de sa carrière, elle avait travaillé sur plus de quatre douzaines d'études cliniques, dont de nombreuses études de grande envergure, mais n'avait jamais vu un environnement de travail aussi « mouvementé » qu'à Ventavia dans l'étude Pfizer.
Je n'ai jamais eu à faire ce qu'on m'a demandé de faire, a-t-elle déclaré au BMJ. Cela semblait juste être quelque chose de différent des choses normales - les choses qui sont autorisées et attendues.
Selon ces sources, les problèmes ont persisté même après la libération de Jackson. L'un d'eux affirme qu'il n'y avait pas assez de personnel à plusieurs reprises pour tester les participants à l'étude qui ont signalé des symptômes de type COVID.
La maladie COVID-19 symptomatique confirmée en laboratoire était le critère d'évaluation principal de l'étude, il s'agissait donc d'une tâche critique. Un mémorandum d'examen de la FDA daté d'août 2021 indique que 477 participants à l'étude suspectés de COVID-19 n'ont pas été testés pour l'infection. "Je ne pense pas qu'il s'agissait de bonnes données propres", a déclaré l'ancien employé de Ventavia à Thacker. "C'est un gâchis fou."
De telles déclarations contredisent clairement les déclarations des dirigeants politiques, des responsables de la santé et des médias grand public. La plupart, comme Le secrétaire australien à la Santé, Greg Hunt, a affirmé que les vaccinations contre le COVID avaient été soumises à des "tests rigoureux et indépendants" pour s'assurer qu'elles étaient "sûres, efficaces et fabriquées selon des normes élevées".
Rien de ce que nous savons jusqu'à présent n'appuie une telle conclusion. Les tests étaient loin d'être rigoureux et non vérifiés de manière indépendante.
Les données du Vaccine Adverse Events Reporting System (VAERS) montrent qu'il est extrêmement peu sûr ; Les données pratiques montrent que l'efficacité diminue en quelques mois et que l'on devient plus sensible aux variantes du SRAS-CoV-2 et à d'autres infections ; et il a été constaté que les normes de fabrication sont également inadéquates car un grand nombre de substances étrangères ont été trouvées dans les flacons.
La science repose sur une collecte de données rigoureuse
La vidéo ci-dessus est un extrait d'une réunion organisée par le sénateur Ron Johnson le 2 novembre 2021, au cours de laquelle Peter Doshi, Ph.D., rédacteur en chef adjoint du BMJ, a souligné certaines des préoccupations de nombreux experts concernant l'intégrité du COVID. données jab expliquées.
Il a souligné que les données brutes de l'étude Pfizer ne seront pas disponibles avant mai 2025. À ce jour, Pfizer a refusé de fournir ses données brutes à des auditeurs indépendants et sans ces données, il n'y a aucun moyen de confirmer que les affirmations de Pfizer sont, en fait, vraies et correctes.
En d'autres termes, on s'attend à ce que nous croyions simplement la parole d'une entreprise qui figure en bonne place sur la liste des criminels en col blanc ; une entreprise a infligé une amende record de 2,3 milliards de dollars en 2009 pour marketing frauduleux et fraude aux soins de santé. Les communiqués de presse ne sont pas scientifiques. Vous commercialisez. Sans les données brutes, nous n'avons aucune base scientifique sur laquelle baser nos décisions concernant le killshot COVID.
Doshi a souligné à quel point le processus que nous suivons est totalement non scientifique. Il souligne également que les médecins ont le devoir éthique de ne pas recommander un traitement pour lequel ils ne disposent d'aucune donnée. Il cite un article de 2020 qu'il a co-écrit :
La transparence des données n'est pas un « bon à avoir ». Les allégations faites sans accès aux données - que ce soit dans des publications évaluées par des pairs ou des prépublications non évaluées par des pairs - ne sont pas des allégations scientifiques.
Les produits peuvent être commercialisés sans accès aux données, mais les médecins et les associations professionnelles doivent déclarer publiquement que sans une transparence totale des données, ils refuseront d'approuver les produits COVID-19 comme étant fondés sur la science.
"Le point auquel je veux en venir est très simple", a déclaré Doshi. « Les données sur le vaccin COVID ne sont pas disponibles et ne le seront pas avant des années. Pourtant, nous ne nous contentons pas de "demander", nous "obligeons" des millions de personnes à prendre ces vaccins... Sans données, ce n'est pas de la science."
La FDA souhaite que les données de l'étude Pfizer soient publiées pendant 75 ans
En septembre 2021, un groupe appelé Public Health and Medical Professionals for Transparency (PHMPT) a déposé une demande de Freedom of Information Act (FOIA) auprès de la FDA pour obtenir les matériaux utilisés pour approuver Comirnaty, y compris les données d'innocuité et d'efficacité, les rapports d'effets indésirables et listes d'ingrédients actifs et inactifs.
Dans sa demande FOIA, le PHMPT a demandé à l'agence d'accélérer la publication des documents - une demande raisonnable étant donné que nous n'avons pas de données brutes et que les vaccins sont administrés aux enfants dès l'âge de 5 ans. Alors que la FDA n'avait toujours pas répondu à la demande de FOIA après un mois, le PHMPT a déposé une plainte.
La FDA a initialement demandé au juge l'autorisation de reporter la publication complète de tous les documents - 329 000 pages au total - jusqu'en 2076 et de ne publier que 500 pages par mois. Le juge a accepté.
Peu de temps après, la FDA a affirmé avoir trouvé 59 000 pages supplémentaires, nécessitant un délai de 20 ans supplémentaires. Selon la FDA, l'autorisation complète ne peut pas avoir lieu avant 2096, date à laquelle la plupart d'entre nous seront morts et enterrés. Comme le note Aaron Siri, l'avocat travaillant sur l'affaire au nom du PHMPT :
Si ce que vous lisez est difficile à croire, c'est parce qu'il est dystopique que le gouvernement donne des milliards à Pfizer, disant aux Américains d'ingérer leur produit, interdisant aux Américains de poursuivre en justice, et refusant pourtant de montrer aux Américains les données sous-jacentes à l'approbation.
En dehors de cela, les 92 pages initialement publiées sont si stressantes que nous n'avons pas besoin de centaines de milliers de pages pour évaluer la sécurité de ces seringues. En fait, les données sont si incroyablement pauvres que l'on doit sérieusement se demander comment la FDA est arrivée à la conclusion que la seringue Pfizer est suffisamment sûre pour être utilisée, en particulier sur les femmes enceintes et les enfants.
Des révélations choquantes dans le premier lot de documents FOIA
À la mi-novembre 2021, deux mois après le dépôt de la plainte, la FDA a publié le premier lot de 91 pages indiquant que la FDA était au courant de problèmes de sécurité choquants au 30 avril 2021.
Au 28 février 2021, Pfizer avait reçu un total de 42 086 rapports d'événements indésirables, dont 1 223 décès, principalement des États-Unis, du Royaume-Uni, d'Italie, d'Allemagne, de France et du Portugal. Parmi ces événements indésirables, 25 379 ont été médicalement confirmés. Le diagramme suivant tiré d'un des documents donne un aperçu général des résultats rapportés.
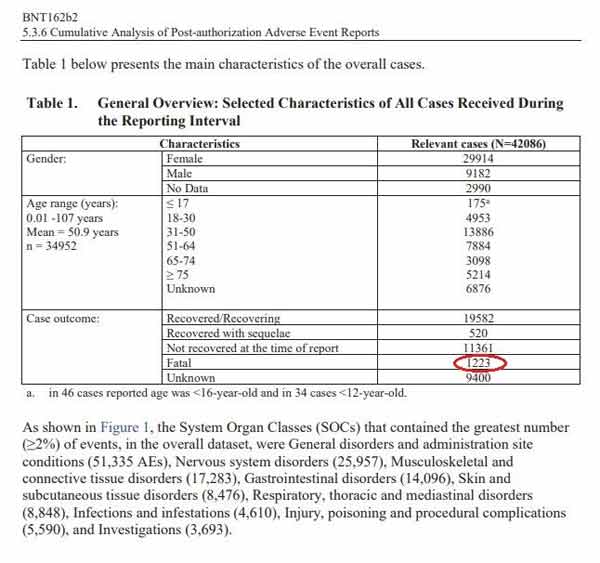
1 223 décès et 42 086 rapports de blessures au cours des trois premiers mois sont un signe clair de sécurité, surtout si l'on considère que le vaccin contre la grippe porcine de 1976 a été retiré après seulement 25 décès.
Dans la vidéo ci-dessus, Melanie Risdon de Western Standard interviewe le Dr. Daniel Nagase, un médecin de l'Alberta, au Canada, qui a été révoqué après avoir traité avec succès des patients COVID-19 avec de l'ivermectine. Nagase discute d'autres données tout aussi dévastatrices dans ces documents.
Il souligne que sur les 42 086 patients qui ont été blessés au cours des trois premiers mois, 520 d'entre eux ont reçu un diagnostic d'invalidité ou de maladie de longue durée. 11 361 n'avaient pas récupéré au moment de la rédaction du rapport. Cela signifie que 27% des personnes blessées ne se sont pas remises de leur incident.
Souvent, lorsque les gens sont blessés par cette injection, ils sont très grièvement blessés. Près d'une personne sur trois qui a reçu l'injection et a subi un effet indésirable est décédée, handicapée de façon permanente ou avec des blessures à long terme non guéries.
Si vous additionnez tout cela : les 1 223 décès, les 520 invalidités de longue durée et les 11 361 qui ne se sont pas remis de leur blessure, cela fait un peu plus de 31 %.
En d'autres termes, près d'une personne sur trois qui a reçu l'injection et a subi un effet indésirable est décédée, handicapée de façon permanente ou avec une blessure non guérie à long terme. "Cela devrait être sur les premières pages", dit Nagase. Comment la FDA peut-elle examiner cela et conclure que la seringue est sûre ? Souvent, lorsque les gens sont blessés par cette injection, ils sont très grièvement blessés.
Les données de Pfizer montrent que la seringue est dangereuse pour les femmes enceintes
Voir la page 12 du document, Analyse cumulative des rapports d'événements indésirables post-autorisation reçus jusqu'au 28 février-2021, pour des données sur les femmes enceintes et allaitantes. Ici aussi, les résultats sont ahurissants et auraient dû déclencher un arrêt complet de la campagne d'injection chez les femmes enceintes et allaitantes.
Il est préoccupant qu'aucune donnée complète n'ait été collectée sur ces femmes, par ex. B. Dans quel trimestre ils étaient lorsqu'ils ont reçu les injections. Cela indique à nouveau de sérieux problèmes avec la collecte de données d'étude par Pfizer. Comment inclure les femmes enceintes dans une étude sans collecter des informations de base, telles que : B. De combien de semaines êtes-vous enceinte ?
À la page 12, on apprend que sur 124 événements indésirables impliquant une femme enceinte, seuls 49 étaient sans gravité et 75 graves. Sur les 274 femmes enceintes qui ont signalé un événement indésirable, 27 % ont subi un événement indésirable GRAVE tel qu'une fausse couche ou une mortinaissance. « C'est un danger incroyable ! » Dit Nagase, et la FDA est également consciente du danger depuis le 30 avril 2021.
Les données montrent également que les mères qui allaitent sont à risque. Sur les 133 mères allaitantes qui ont soumis un rapport, 17 des nourrissons allaités - 13% - ont subi un événement indésirable à cause de cette exposition secondaire (lait maternel), un résultat que Nagase décrit comme "absolument incroyable".
Donc l'idée que le « vaccin » se transmet par le lait maternel est absolument vraie », dit-il. « Cela est démontré par les propres données de Pfizer sur les événements indésirables
Enfants à risque de blessures graves à long terme
Pfizer a également reçu 34 rapports d'événements indésirables chez des enfants de moins de 12 ans, le plus jeune enfant ayant 2 mois. Parmi ceux-ci, 24 ont été classés comme "graves" et seulement 10 comme "pas sérieux". Ainsi, parmi les enfants qui ont été blessés, 70,6 % ont subi des blessures GRAVES.
Comment nos autorités sanitaires peuvent-elles approuver cette seringue COVID pour les enfants de moins de 12 ans alors que la grande majorité des blessures, si elles le font, sont graves ? De plus, 13 des enfants grièvement blessés n'avaient toujours pas été soignés au 28 février 2021.
De l'avis de Nagase, la seringue COVID de Pfizer aurait dû être définitivement retirée du marché sur la base de ces seuls documents. La raison pour laquelle cela ne s'est pas produit, à son avis, est que les systèmes médicaux et réglementaires ont été corrompus et usurpés par l'industrie pharmaceutique. Ils veulent que ces seringues rapportent de l'argent, et nos autorités sanitaires couvrent les dommages avérés pour alimenter la recherche du profit.
En fin de compte, vous seul pouvez décider vous-même de ce qui est dans votre meilleur intérêt. Mais veuillez lire les dernières preuves scientifiques avant de prendre votre décision et ne faites pas aveuglément confiance aux communiqués de presse des entreprises et aux déclarations de sécurité non fondées.
Les propres données de Pfizer prouvent que, selon toute définition raisonnable du mot, il n'est pas sûr, en plus de ce que Jackson et d'autres ont vu qui ont vu à quel point la collecte de données est bâclée.
Sources:
- 1, 3, 8 Le BMJ 2021 ; 375 : n2635
- 2 Le dernier vagabond américain 2 décembre 2021
- 4 Facebook Pfizergate
- 5 Ilussidario.net Pfizergate
- 6 Covidvaccinereaction.com
- 7 Le BMJ 2021 ; 375 : n2635 Réponse rapide
- 9 Twitter Greg Hunt 15 février 2021
- 10 CNBC 30 août 2021
- 11 ABC Australie 4 septembre 2009
- 12 Le BMJ 2020 ; 370 ; m3260
- 13 Le défenseur 19 novembre 2021
- 14, 15 Newsmax 8 décembre 2021
- 16 documents Pfizer de PHMPT.org
- 17 thekylebecker.substack.com 21 novembre 2021
- 18, 19 Analyse cumulative des rapports d'événements indésirables post-autorisation reçus jusqu'au 28 février-2021




